MICI et traitements non médicamenteux
Article
Publié le 16/11/2022
Information proposée par Association François Aupetit - Crohn RCH France
L’arsenal thérapeutique pour les maladies inflammatoires chroniques de l’intestin (MICI) ne cesse d’évoluer.
Non seulement de nouvelles molécules sont en cours d’étude mais aussi de nouvelles modalités non médicamenteuses de prise en charge pourraient intégrer cet arsenal dans les prochaines années.
Trois modalités sont étudiées actuellement : l’aphérèse leucocytaire (granulocytes et monocytes), la neurostimulation vagale (NSV) et la transplantation du microbiote fécal (TMF).
Neurostimulation vagale
Notre tube digestif est relié au cerveau par des millions de neurones via le nerf vague. Un chercheur américain, Dr Kevin Tracey, a mis en évidence des propriétés anti-inflammatoires de ce nerf. Ces propriétés pourraient être activées par des stimulations électriques afin de contrôler l’inflammation. Fort de ces constats, des études sont réalisées actuellement en France afin de mettre en avant le rôle de cette stimulation du nerf vague dans les MICI et la maladie de Crohn notamment.
Le nerf vague est un nerf crânien reliant le cerveau aux organes du corps, dont le système digestif. Par son biais, le cerveau et les intestins entretiennent une relation privilégiée sous la forme d’un réseau de communication à double sens : l’axe neuro-digestif. Le cerveau est tenu au courant en permanence de l’état digestif, de l’activité du microbiote et des cellules immunitaires intestinales. En retour, le cerveau régule la digestion et peut déclencher des réactions immunitaires de défense.
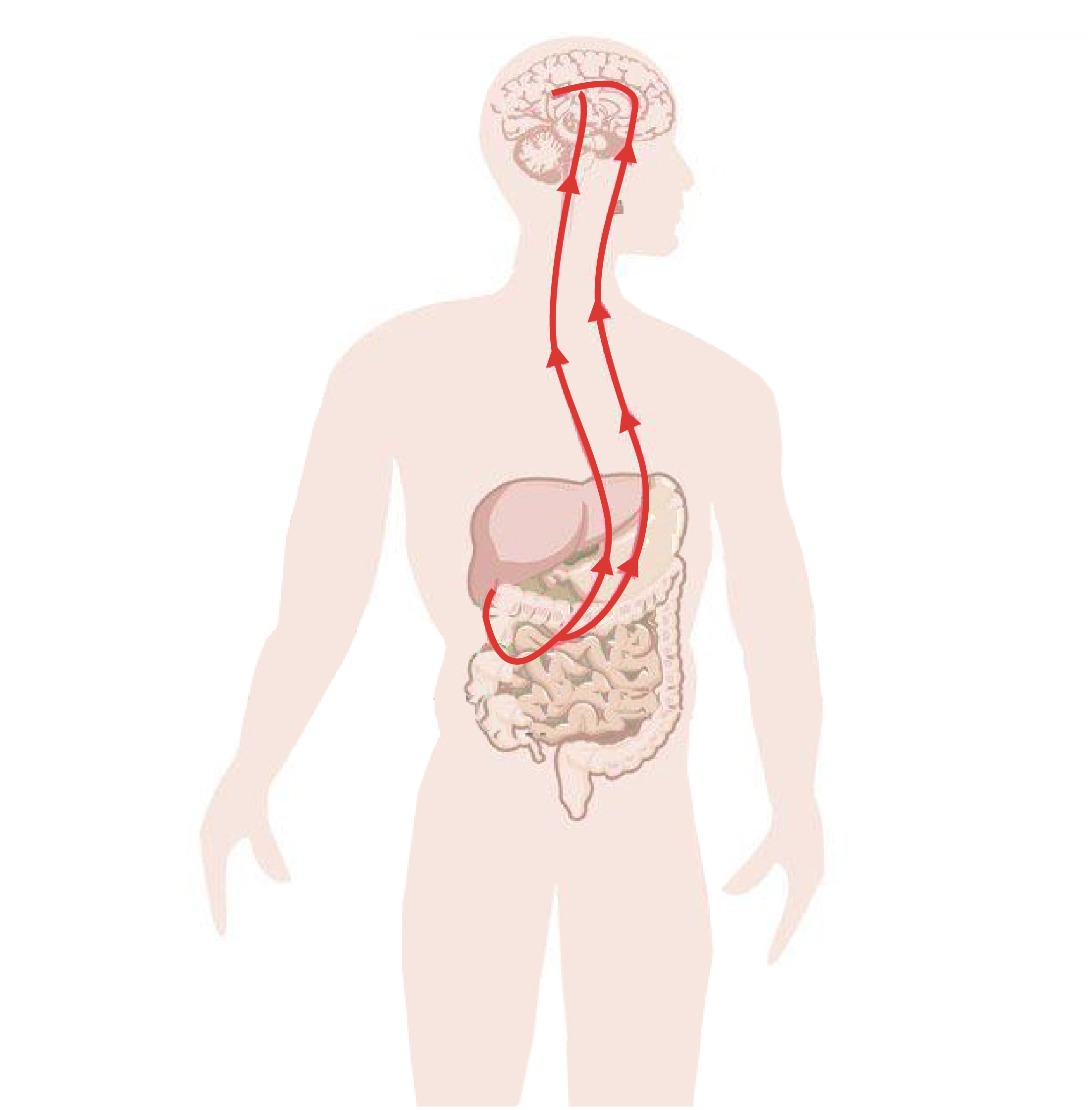
Des dysfonctionnements de cet axe neuro-digestif seraient corrélés au syndrome de l’intestin irritable et aux maladies inflammatoires chroniques de l’intestin (MICI). La stimulation de ce nerf vague – afin de retrouver une activité normale – est donc une piste thérapeutique dans la maladie de Crohn comme dans la RCH (rectocolite hémorragique). Selon Dr Kevin Tracey, le nerf vague serait le « bouton off » de l’inflammation.
La neurostimulation vagale (NSV) consiste en une stimulation électrique, fréquente et de faible intensité, du nerf vague. Pour cela, un fin filament est implanté autour du nerf vague dans le cou. Ce filament est relié à un générateur glissé sous la clavicule. Ce même générateur va émettre des impulsions électriques – toutes les 5 minutes par exemple – pour stimuler le nerf et potentialiser son rôle anti-inflammatoire.
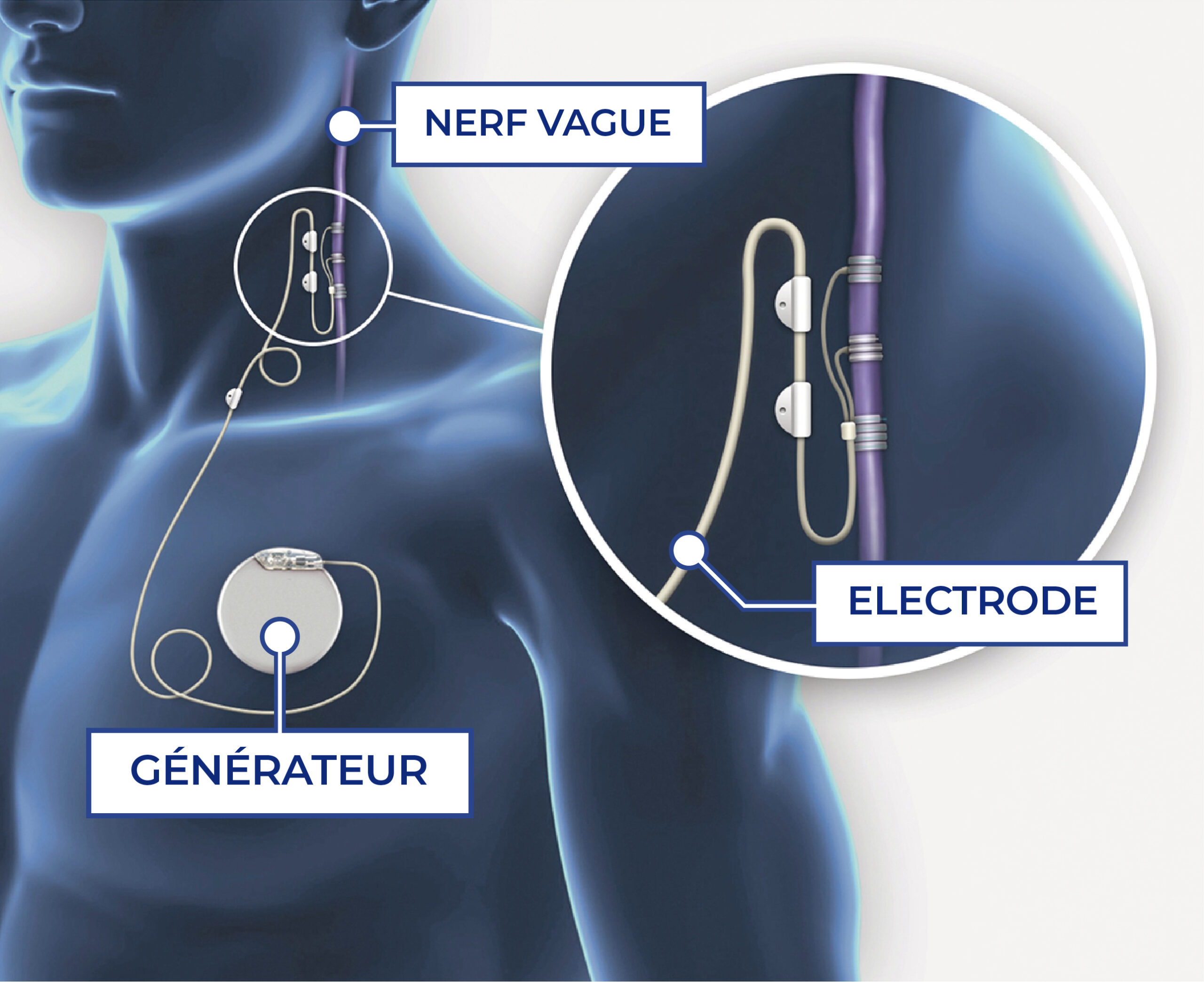
Ainsi, le Pr Bruno Bonaz, au CHU Grenoble-Alpes, a mis en place une étude sur l’efficacité de la neurostimulation vagale sur 9 patients atteints de la maladie de Crohn. Les résultats sont encourageants : 6 patients sont en rémission avec cicatrisation des lésions depuis l’implantation en 2012. L’effet n’est pourtant pas immédiat, il faut attendre 2-3 mois avant d’observer une amélioration des symptômes.
Les patients traités témoignent d’une diminution significative de la douleur associée à un regain d’énergie. Ils rapportent aussi que la voix peut devenir transitoirement rauque pendant les courtes périodes de stimulation électrique.
En résumé, cette méthode apparait comme une alternative aux médicaments ou un complément des traitements existants afin d’en réduire les doses. Des études de plus grande envergure sont attendues afin de confirmer ces premiers résultats positifs et de déterminer avec précision les modalités d’utilisation – intensité et fréquence de stimulation.
Aphérèse leucocytaire
Les maladies inflammatoires chroniques de l’intestin (MICI) sont caractérisées, entre autres, par une activation inappropriée du système immunitaire et un syndrome inflammatoire. Les leucocytes sont une des pierres angulaires de cette pathogénèse.
Ces leucocytes – ou globules blancs – sont les cellules immunitaires, que l’on retrouve dans le sang. Elles ont un rôle principal dans les réactions de défense de l’organisme et sécrètent des cytokines, molécules-messagers de l’inflammation. Parmi ces cytokines, on retrouve les interleukines et les TNF (tumor necrosis factor).
Les traitements immunodépresseurs et les biothérapies anti-TNFα consistent à intercepter ces cytokines afin de réduire l’inflammation et arrêter l’emballement immunitaire.
Et si on revenait à la source directement en visant les leucocytes et en les éliminant du sang ?
C’est la solution avancée par l’aphérèse dite GMA (Granulocytes/Monocytes Apheresis). L’aphérèse est une technique de prélèvement de certains composés du sang par un système de circulation extracorporelle. Il en existe différentes sortes :
- Plasmaphérèse : permettant de séparer le plasma du reste,
- Leucaphérèse : permettant de prélever uniquement les globules blancs
- Thrombaphérèse : permettant de prélever uniquement les plaquettes.
En savoir plus
Le sang se compose de cellules flottant dans un liquide aqueux : le plasma. Parmi ces cellules, on retrouve majoritairement les globules rouges, les globules blancs et les plaquettes.
Chaque type de cellules présente des particularités propres et des fonctions différentes :
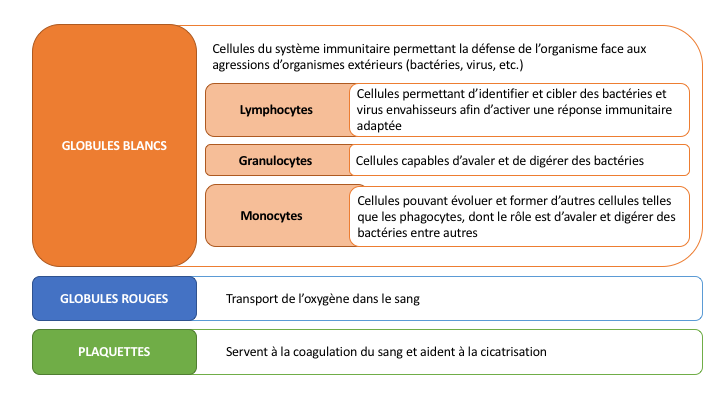
L’aphérèse thérapeutique par adsorption de granulocytes et monocytes /macrophage est une aphérèse du sang total avec circulation extracorporelle par le biais de deux ponctions veineuses : une dans chaque bras.
Lors de l’aphérèse, le patient est perfusé et son sang passe dans une colonne qui sépare les différents composés du sang par différentes techniques : adsorption, centrifugation ou extraction des composés sur les billes adhésives, grâce à un moniteur qui assure le rôle de pompe. Après séparation, le sang libéré de ces cellules inflammatoires est réinjecté au patient.
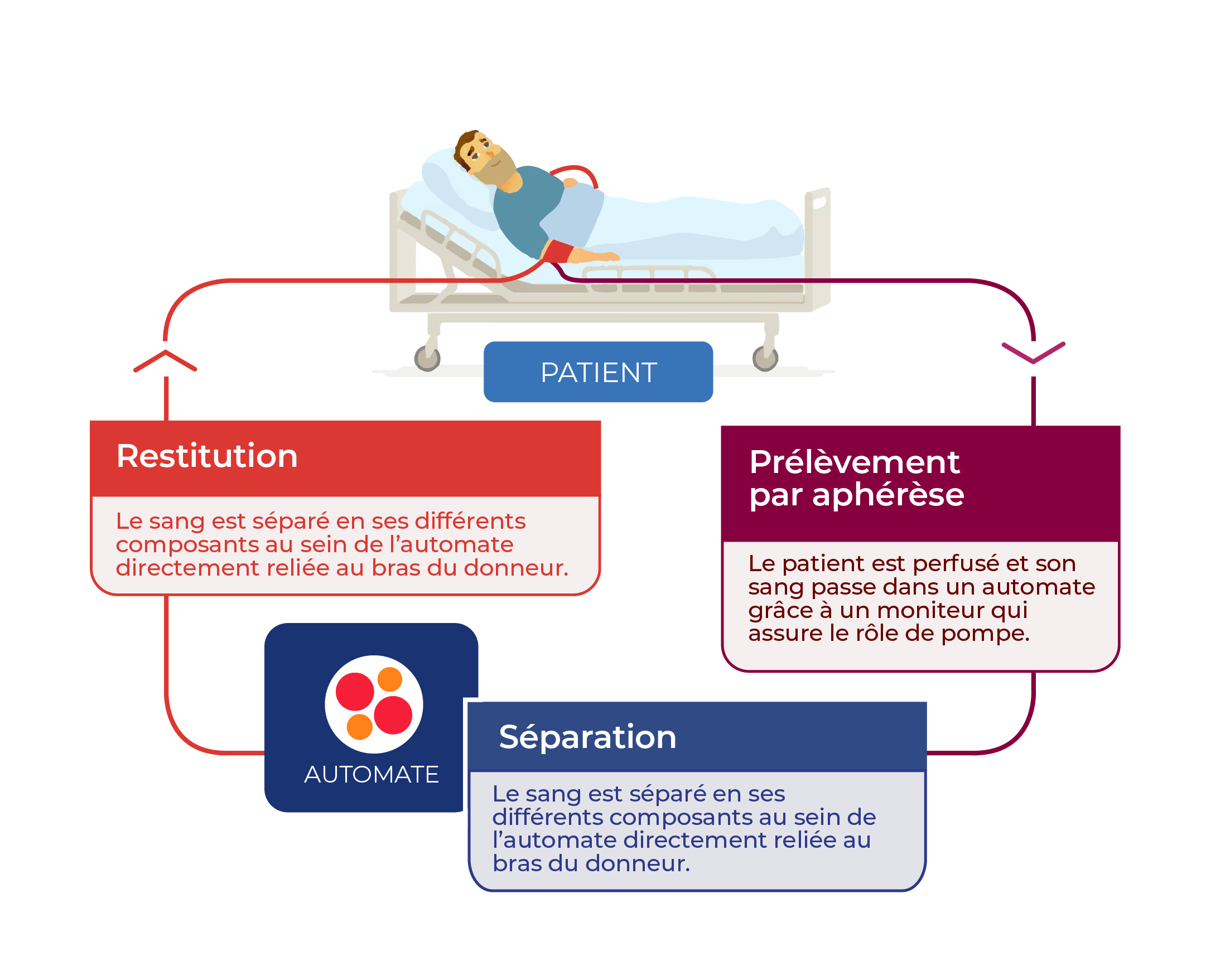
Dans la GMA, on s’intéresse en particulier aux granulocytes, monocytes et macrophages (sans toucher aux lymphocytes). Ainsi, ces cellules immunitaires sont extraites du sang et le sang « épuré » est réinjecté au patient. Le but ici est de supprimer la fraction pathologique du sang : les granulocytes, monocytes et macrophages responsables de l’activation inadaptée du système immunitaire et du syndrome inflammatoire.
Cette méthode est mise à l’épreuve chez des patients atteints de maladie de Crohn (MC) et des patients atteints de RCH (rectocolite hémorragique). De nombreuses études au niveau international montrent des résultats encourageants : cohorte de 230 patients (RCH + MC) en Italie, étude scandinave avec 100 patients (RCH + MC), étude prospective au Japon (656 patients RCH) etc.
Typologie des patients intégrés dans les études :
- Patients corticodépendants,
- Patients avec une réponse insuffisante ou intolérants aux traitements immunosuppresseurs ou anti-TNF alpha.
De manière globale, l’aphérèse est bien tolérée, avec peu d’effets indésirables. Les résultats restent hétérogènes, certaines études montrent des effets bénéfiques significatifs sur la rémission et la disparition des symptômes tandis que d’autres ne montrent pas d’écart d’efficacité significatif entre cette méthode et un placebo.
Globalement, une meilleure efficacité est toutefois observée dans la RCH pour l’induction d’une rémission, par rapport à la maladie de Crohn.
En conclusion, la GMA pourrait être une option non médicamenteuse pour le traitement des MICI, surtout en cas de maladie réfractaire et d’échec des traitements médicamenteux conventionnels.
Des études complémentaires pourront détailler la mise en œuvre de cette méthode : fréquence des séances, durée de traitement et profils de patients concernés.
Transplantation fécale
Une cause est régulièrement évoquée dans l’apparition et le développement des MICI (maladies inflammatoires chroniques de l’intestin) : un déséquilibre du microbiote intestinal. Les chercheurs tentent donc de percer le mystère du microbiote intestinal, de comprendre son fonctionnement, de trouver des techniques pour le moduler et corriger la dysbiose. Une piste avancée est la transplantation du microbiote fécal (TMF). En quoi consiste-t-elle ?
La transplantation du microbiote fécal ou bactériothérapie fécale « consiste à introduire les selles d’une personne saine dans le tube digestif d’un patient afin de reconstituer sa flore intestinale et de l’aider à lutter contre des bactéries pathogènes ».
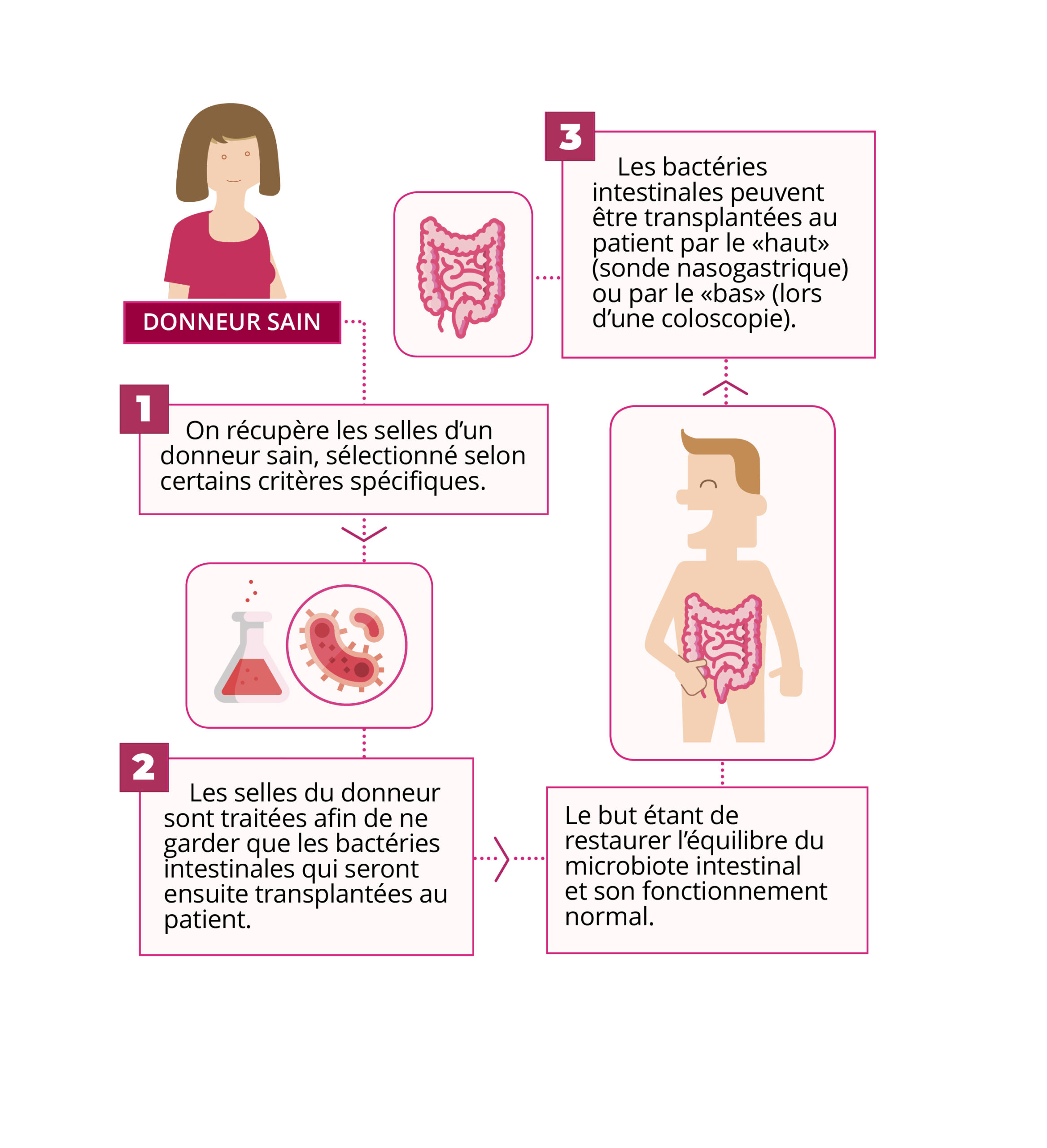
Afin de limiter les risques infectieux liés à la TMF, les donneurs sains font l’objet d’une stricte sélection et doivent répondre à certains critères : absence de pathologies chroniques, absence de traitement médicamenteux au long terme, pas de traitement antibiotique récent, dépistage négatif aux agents infectieux, entre autres.
A la suite de cette sélection, les selles des donneurs sont récoltées puis conservées afin de réaliser les tests nécessaires – ce qui nécessite un délai entre la collecte et la transplantation. Ensuite, elles sont préparées avec du sérum physiologique et filtrées avant d’être conditionnées pour leur administration au patient.
Cette administration peut s’effectuée par lavement ou vaporisation de la solution préparée lors d’une coloscopie ou par sonde nasogastrique. Une autre voie d’administration envisagée est la prise de gélules contenant les selles congelées ou lyophilisées.
Actuellement, la transplantation fécale est indiquée uniquement dans les infections récidivantes à Clostridium difficile – qui est une bactérie particulièrement agressive. La méthode a démontré son efficacité dans diverses études, au niveau européen et nord-américain : l’administration de bactéries fécales a permis de restaurer le microbiote intestinal perturbé par l’infection et de casser le cycle des infections récidivantes.
Ces preuves d’efficacité ont favorisé de nouvelles recherches dans d’autres pathologies telles que les maladies inflammatoires chroniques de l’intestin (MICI). Ainsi, l’équipe du Pr Sokol à l’hôpital Saint-Antoine cherche à prouver un impact favorable de ce remplacement de microbiote sur l’évolution de la RCH.
Pour plus d’informations vous pouvez consulter l’article sur cette étude « Impact de la transplantation fécale sur le microbiote dans la maladie de Crohn ».
Outre l’efficacité de la méthode, d’autres questions restent non résolues. Comment bien sélectionner les donneurs ? Comment les échantillons de selles doivent-ils être préparés ? Comment apprêter le receveur à la transplantation ? Vaut-il mieux administrer le microbiote par voie haute ou par voie basse ? La TMF est-elle efficace lors des poussées ou pour maintenir la rémission ?
Les études devront aussi explorer la sécurité de cette méthode au long terme. La transplantation de microbiote fécal peut-elle transmettre des maladies infectieuses ou des pathologies chroniques ?
La TMF ouvre donc de nouvelles pistes de recherche dans le traitement des MICI et la voie orale semble être une alternative particulièrement prometteuse. De nombreuses études pilotes expérimentent l’utilisation de gélules renfermant des excréments congelés dans le traitement de bactéries résistantes. L’efficacité semble être similaire entre les deux modes d’administration tout en conférant un meilleur confort d’utilisation avec les gélules.
Des résultats prometteurs seront à développer afin d’espérer compter un jour ce type de traitement dans l’arsenal thérapeutique des MICI, d’ici 5 à 10 ans.
Les autres traitements non médicaux :
À retrouver sur https://www.afa.asso.fr/maladie-inflammatoire-chronique-de-linstestin/se-soigner/traitements-non-medicamenteux-mici/
L’afa est aujourd’hui l’unique organisation française, reconnue d’utilité publique, à se consacrer aux Maladies Inflammatoires Chroniques Intestinales (MICI), maladie de Crohn et rectocolite hémorragique.
L’association s’est donnée plusieurs missions :
- guérir en soutenant des programmes de recherche fondamentale et clinique, en proposant des améliorations dans le parcours de soins et en produisant des connaissances sur nos maladies ou sur le "vivre avec" ;
- informer et soutenir les malades et leurs proches via un réseau de professionnels et de bénévoles formés répartis sur 22 régions et nos outils internet ;
- partager son expérience avec les autres malades et leurs proches sur internet ou lors de rencontres locales ;
- représenter tous les malades ainsi que leurs proches, porter leurs voix auprès des décideurs politiques et de santé ;
- former et informer les professionnels de santé sur le quotidien avec la maladie ;
- communiquer sur nos maladies encore beaucoup trop méconnues et tabous ;
- agir en tant qu'acteur de santé publique dans la démocratie sanitaire.
Association François Aupetit - Crohn RCH France
