Endométriose colo-rectale : comment la diagnostiquer ?
Article
Publié le 16/05/2022
Information proposée par Association Française de Formation Médicale Continue en Hépato-Gastro-Entérologie (FMCHGE)
Les cinq points à retenir
- L’endométriose colorectale concerne environ 15 % des patientes atteintes d’endométriose profonde ; elle en est une forme particulière.
- Le diagnostic d’endométriose profonde et celui d’atteinte colorectale sont suspectés sur des signes cliniques ; ils doivent être confirmés par l’imagerie non invasive (échographie trans vaginale, IRM pelvienne, échoendoscopie rectale).
- Le retentissement peut être majeur sur la qualité de vie en raison des douleurs et de l’infertilité.
- La prise en charge repose avant tout sur le traitement médical ; elle doit être assurée par une équipe pluridisciplinaire, supervisée par un centre expert. La chirurgie est nécessaire en cas de lésions colorectales occlusives, d’absence d’efficacité des traitements médicaux, et de complications imposant un geste urgent ; la coelioscopie à visée purement diagnostique est à déconseiller.
- L’échoendoscopie rectale peut être utile au diagnostic d’atteinte colo-rectale ; elle s’intègre dans le cadre d’un bilan préopératoire.
Endométriose colo-rectale, circonstances de découverte, symptômes et présentation clinique
L’expression clinique de l’endométriose profonde est extrêmement diverse et marquée par une absence de « parallélisme anatomo-clinique ». Elle est très souvent brouillée par la coexistence d’un syndrome de l’intestin irritable (8-10). Les patientes atteintes d’endométriose colo-rectale, même si elles ont statistiquement plus souvent des douleurs à la défécation et une constipation cyclique(Tableau 2), expriment surtout les symptômes communs aux localisations profondes postérieures : (ils constituent les classiques « 4 D » : dysménorrhées, dyspareunies, douleurs abdominales non cycliques, et dyschésie. L’interrogatoire doit renseigner sur l’existence de dyschésie, de ténesme, et/ou de douleurs à la défécation uniquement présentes ou majorées en période de règles. Le syndrome (sub)occlusif peut faire suspecter une atteinte digestive sténosante, présente chez 8 à 25 % des patientes ayant une endométriose digestive (7, 9, 10), mais il peut également survenir par le biais d’adhérences surtout chez des patientes préalablement opérées. Quant aux ménorragies, elles ne sont pas un signe d’endométriose profonde mais elles font davantage évoquer une adénomyose, fréquemment associée, et majorant les douleurs cycliques (11, 12). Schématiquement (13), 5 principales situations conduisent au diagnostic d’endométriose profonde :
- l’exploration de dysménorrhées parfois anciennes et n’ayant pas encore fait évoquer le diagnostic,
- la prise en charge d’une infertilité (l’endométriose affecterait 25 à 50 % des femmes infertiles, et la fertilité par cycle est abaissée chez les patientes endométriosiques : 2-10 %, comparée à celle de la population des femmes en âge de procréer : 15-20 %) (14, 15),
- le constat d’endométriomes ovariens sur une échographie de routine amenant à rechercher une endométriose profonde (d’autant plus fréquemment associée que les kystes sont bilatéraux volumineux et symptomatiques),
- la survenue d’un épisode douloureux aigu ayant conduit la patiente aux urgences hospitalières,
- l’information sur l’endométriose notamment médiatique, croissante depuis quelques années, ou tout simplement le « bouche à oreille ».
Signes cliniques d’endométriose profonde
- Dysménorrhées
- Dyspareunies profondes posturales
- Douleurs pelviennes chroniques inter-menstruelles (symptôme plus tardif dans son installation parfois décrit par les patientes comme une prolongation des dysménorrhées au-delà de la période des règles)
- Infertilité (rôle possible de l’adénomyose souvent associée)
Signes digestifs pouvant faire évoquer une atteinte colorectale (signes non spécifiques)
- Troubles du transit divers (en lien avec l’inflammation due aux micro-hémorragies intra pariétales)
- Dyschésie - Douleurs digestives Ténesme
- Rectorragies cycliques (non significatives)
- Occlusion
Tableau 2 : Les symptômes digestifs de l’endométriose profonde sont-ils spécifiques des atteintes colorectales ? Étude comparative sur 3 groupes de patientes (Roman et al Human reprod 2012)
| Endométriose Péritonéale n = 21 | Endométriose profonde sans atteinte digestive n = 32 | Endométriose profonde avec atteinte digestive n = 83 | |
| Douleurs défécation cycliques | 38 % | 42,9 % | 67,9 % |
| Constipation cyclique | 33 % | 26,2 % | 54,7 % |
En pratique courante, l’atteinte endométriosique colo-rectale est volontiers diagnostiquée dans 2 populations distinctes :
1/ Des femmes jeunes, aux alentours de la trentaine, traitées par contraception orale depuis plusieurs années, et qui ayant interrompu cette prescription pour un projet de grossesse, voient survenir, réapparaître, ou s’aggraver des symptômes antérieurement absents, ou correctement contrôlés par le contraceptif ; les dyspareunies sont le principal motif de consultation et les signes digestifs, au second plan, ne sont en fait retrouvés que par l’interrogatoire orienté.
2/ Des femmes plus âgées ayant déjà alterné des périodes de contraceptions hormonales et des grossesses et qui souhaitent interrompre la contraception orale au profit d’un dispositif intra-utérin ; les symptômes d’endométriose surviennent alors, puis s’aggravent avec apparition de signes digestifs de plus en plus nets. L’examen physique gynécologique peut poser le diagnostic d’endométriose profonde, mais il ne permet pas de faire un bilan d’extension précis ni de certifier le diagnostic d’atteinte digestive (13).
Ces localisations digestives peuvent également concerner des profils moins classiques (adolescentes, femmes ménopausées, patientes ayant déjà été opérées), ou même être constatées chez des malades ne présentant pas de douleur ni de symptôme digestif (7, 8, 16). Le recours large à l’imagerie est donc recommandé, ce d’autant qu’elle peut contribuer à l’élaboration de scores diagnostiques et prédictifs. Les plus récents d’entre eux reposent surtout sur des critères cliniques qui peuvent être recueillis à l’interrogatoire ou à partir de questionnaires, et sur une imagerie de première ligne. En voie de validation, ces scores sont très prometteurs pour réduire les délais diagnostiques de l’endométriose, préciser son phénotype (péritonéale, ovarienne ou profonde), prédire le risque d’atteinte colo-rectale, et optimiser ainsi la prise en charge des patientes (12, 17, 18).
Imagerie de l’endométriose profonde, diagnostic et bilan d’extension des formes colo-rectales
L’imagerie est incontournable dans le diagnostic et le bilan d’extension de l’endométriose profonde, notamment pour certifier et décrire les éventuelles infiltrations colo-rectales, celles-ci étant de nature à majorer la symptomatologie et surtout à « complexifier » le geste opératoire en cas d’intervention. Trois principaux examens sont couramment utilisés pour cela : l’échographie trans-vaginale (ETV), l’imagerie par résonnance magnétique (IRM) et l’écho-endoscopie rectale (EER) ; les performances de chacune de ces techniques varient selon les localisations évaluées (16, 19-21). L’IRM permet l’examen le plus complet, avec en particulier une bonne exposition du torus et des ligaments utéro-sacrés et la visualisation des atteintes vésicales. Avec des sensibilités et spécificités de 94 % et 77 %, pour le diagnostic d’endométriose profonde, elle est donc aujourd’hui largement prescrite en cas de suspicion clinique ou échographique, mais également pour le bilan d’extension et la surveillance évolutive. Beaucoup d’études en ont évalué la méthodologie et les performances (20-24).
L’ETV offre une excellente description des ovaires, et par une séméiologie dynamique, elle permet de suspecter les adhérences et de décrire certaines infiltrations digestives (5). Plusieurs équipes expertes dans la prise en charge de l’endométriose ont d’ailleurs considéré l’ETV comme l’examen morphologique de première ligne (5, 25), et Holland et al ont montré qu’elle pouvait décrire très correctement les atteintes colorectales (26). Un protocole d’examen précis est désormais recommandé aux opérateurs effectuant cet examen : réaliser avant tout un « balayage » de l’utérus, des ovaires et du cul-de-sac de Douglas, pour ensuite rechercher les adhérences et les signes indirects d’endométriose profonde, avant de décrire celle-ci en détail (5).
Les bonnes performances de ces experts ne sont toutefois pas toujours atteintes en pratique courante comme a pu le montrer un travail récent (27). Dans cette étude observationnelle des performances de l’ETV dans le bilan préopératoire de l’endométriose profonde, 115 patientes avaient été incluses, dont la moitié seulement avait été examinée par un échographiste expert. Les opérateurs qualifiés obtenaient des sensibilités et spécificités de 40 et 90 % pour le diagnostic d’atteinte colorectale, mais les autres échographistes, moins expérimentés, n’avaient pas repéré les atteintes colo-rectales présentes. De fait, celles-ci sont surtout accessibles à l’EER, qui décrit aussi très correctement les atteintes de la cloison recto-vaginale (ou septum) définies par les atteintes sous-péritonéales situées en dessous du bord postéro-inférieur du col utérin.
Cette technique aux mains des gastroentérologues a initialement été évaluée pour le diagnostic de l’endométriose colo-rectale dans les années 1990, d’abord par des séries ouvertes, surtout rétrospectives (29-34), puis par d’autres comparant l’EER avec l’IRM et l’ETV (16, 24, 35, 36). Très tôt, en particulier dans le travail réalisé à l’hôpital Cochin (tableau 5), il avait été constaté, avec l’EER, de bonnes sensibilités et valeurs prédictives négatives pour le diagnostic des atteintes colo-rectales, supérieures à celles des autres techniques. Cela n’a jamais été démenti par la suite, et la complémentarité des 3 techniques a pu être affirmée notamment dans le bilan d’extension pré opératoire par 2 méta-analyses (20, 23).
Tableau 5 : Étude Chapron 2004, comparaison IRM et EER pour le diagnostic des atteintes colo-rectales 81 patientes opérées (34 avec atteinte digestive) (se : sensibilité, sp : spécificité, vpp : valeur prédictive positive, vpn : valeur prédictive négative)
| Se | Sp | Vpp | Vpn | |
| IRM | 76,5 % | 97,9 % | 96 % | 85,2 % |
| EER | 97,1 % | 89,4 % | 86,8 % | 97,7 % |
À partir d’un travail récent réalisé à l’hôpital Tenon sur 407 patientes (37), il a bien été montré que pour le diagnostic de l’atteinte colorectale, l’utilisation combinée de l’IRM et de l’EER (aucun des deux opérateurs n’ayant connaissance des résultats de « l’autre imagerie »), augmentait la sensibilité de 10 %. En pratique, lorsque les 2 techniques étaient concordantes pour l’atteinte colo-rectale, celle-ci était confirmée en per opératoire dans 100 % des cas. En revanche, lorsqu’une seule des deux était en faveur de l’infiltration digestive, elle était confirmée 6 fois sur 10 (l’EER ayant ici une supériorité diagnostique sur l’IRM : 66 % vs 48 %).
Lorsqu’elle est pratiquée avec un écho-endoscope radial et selon une méthodologie codifiée, l’EER est très performante (38). L’examen est réalisé en une vingtaine de minutes après un lavement normacolR, le recours à l’anesthésie générale étant plutôt limité aux patientes anxieuses ou spontanément très algiques ; chez les autres, des explications claires et rassurantes contribuent à la bonne tolérance. Si possible, afin de ne pas insuffler d’emblée, le « temps endoscopique » est réalisé après le « temps échographique ». Celui-ci repose sur une méthodologie proche de celle décrite avec l’ETV. Ainsi, une fois la sonde placée au-dessus du sigmoïde, un premier temps de balayage d’ensemble vérifie l’aspect de l’utérus et des ovaires, la présence ou non d’un épanchement liquidien du cul de sac de Douglas et de signes d’adhérences ou d’infiltrations digestives.
Les signes indirects d’endométriose profonde les plus courants sont le caractère rétracté des ovaires vers la ligne médiane, la fixité de l’utérus et la présence d’endométriomes ovariens (39). Ceux-ci, on l’a vu, sont d’autant plus souvent associés à un contexte d’endométriose profonde qu’ils sont bilatéraux et de grande taille.
La recherche à proprement parler des atteintes digestives impose un examen soigneux et exhaustif de la stratification échographique pariétale. La paroi peut être épaissie avec disparition ou persistance des couches échographiques. Dans le premier cas, l’épaississement de la musculeuse est évocateur d’endométriose rectale et/ou sigmoïdienne tandis que si la musculeuse reste très peu épaissie et faisant plutôt partie d’une véritable « attraction » de la paroi vers le nodule profond au niveau du torus ou des ligaments utéro-sacrés, on évoque davantage une simple adhérence (figures 3-6).
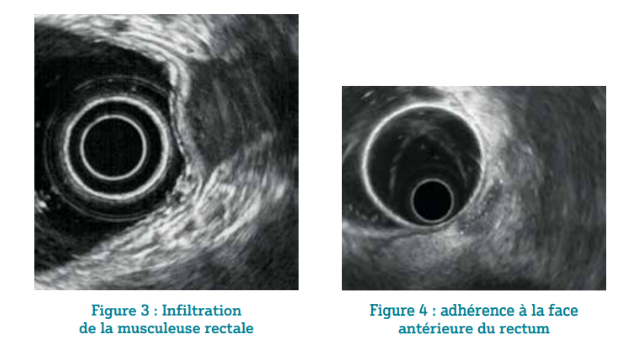
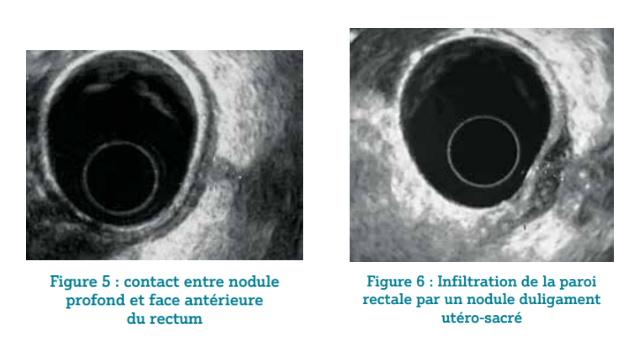
Plusieurs passages de l’écho-endoscope depuis le sigmoïde distal jusqu’au bas rectum sont nécessaires pour aboutir à ces conclusions, et l’instillation d’eau dans la lumière digestive et dans le ballonnet placé autour de la sonde aide au repérage et à la description des lésions, en particulier celle du sigmoïde.
L’aspect de ces lésions et leurs dimensions en épaisseur diamètre et circonférence sont notés, tout comme la distance entre le pôle inférieur de la lésion la plus distale et le plancher pelvien. Il convient également avant de retirer la sonde, de déterminer le caractère intègre du canal anal, ou l’existence d’éventuels « défects » en lien avec des antécédents de chirurgie anale ou d’accouchement par voie basse.
L’EER est donc le plus souvent proposée dans le bilan d’extension locorégionale de l’endométriose profonde lorsqu’une atteinte digestive est suspectée, particulièrement si elle n’a pas été repérée ou correctement décrite par les autres imageries. Sa place est surtout importante dans le bilan préopératoire ; en raison d’une bonne valeur prédictive négative, elle est fiable lorsqu’il s’agit d’écarter le diagnostic d’atteinte colo-rectale pour anticiper la nature et la durée du geste chirurgical. Cependant ce n’est qu’une fois tous les résultats d’imagerie à disposition qu’il devient réellement possible de répondre aux questions que soulève la présence d’une infiltration colo-rectale (tableau 6).
Tableau 6 : Principales questions auxquelles l’imagerie se doit de répondre chez les patientes atteintes d’endométriose profonde
|
1. Existe-t-il une atteinte digestive en particulier colorectale ? 2. Quelle en est la taille ? 3. Est-elle responsable d’une sténose ? 4. Quelle est la profondeur de l’atteinte dans la paroi ? 5. Quelle est la distance entre le pôle inférieur de l’atteinte et la marge anale ? |
|
La réponse à ces questions incontournables aide à préciser au mieux :
|
Test de connaissances
Nous vous invitons à tester vos connaissances sur l’ensemble des QCU (Questionnaire à Choix Unique) de www.fmcgastro.org : testez ici vos connaissances sur le sujet.
Références
- 1. Weed JC, Ray JE. Endometriosis of the bowel. Obstet Gynecol 1987; 69:727–30.
- 2. Wills HJ, Reid GD, Cooper MJ, Morgan M. Fertility and pain outcomes following laparoscopic segmental bowel resection for colorectal endometriosis: a review. Aust NZJ Obst Gynecol. 2008; 48(3): 292-5. doi :10.1111/j.1479- 828X.2008.00871.x
- 3. Donnez J, Nisolle M, Gillerot S, Smets M, Bassil S, Casanas-Roux F. Rectovaginal septum adenomyotic nodules: a series of 500 cases. Br J Obstet Gynaecol. 1997 Sep;104(9):1014-8
- 4. Chapron C, Fauconnier A, Vieira M, et al. Anatomical distribution of deeply infiltrating endometriosis, surgical implications and proposition for a classification, Human Reprod 2003;18:157-61.
- 5. Guerriero S, Condous G, Van den Bosch T, et al. Systematic approach to sonographic evaluation of the pelvis in women with suspected endometriosis, including terms, definitions and measurements: a consensus opinion from the International Deep Endometriosis Analysis (IDEA) group. Ultrasound Obstet Gynecol. 2016 Sep;48(3):318-32. doi: 10.1002/ uog.15955. Epub 2016 Jun 28.
- 6. Kamergorodsky G, Ribeiro PA , Galvao MA, Abrao MS, Donadio N, et al. Histologic classification of specimens from women affected by superficial endometriosis, deeply infiltrating endometriosis, and ovarian endometriomas Fertil Steril 2009; 92: 2074–2077.
- 7. Meuleman C, Tomassetti C, D’Hoore A, Van Cleynenbreugel B, Penninckx F, et al. Surgical treatment of deeply infiltrating endometriosis with colorectal involvement. Hum Reprod Update. 2011 May-Jun;17(3):311-26. doi: 10.1093/ humupd/dmq057. Epub 2011 Jan 13.
- 8. Ek M, Roth B, Ekström P, Valentin L, Bengtsson M, et al. Gastrointestinal symptoms among endometriosis patients - A case-cohort study. BMC Womens Health. 2015 Aug 13;15:59. doi: 10.1186/ s12905-015-0213-2.
- 9. Roman H, Prise en charge de l’endométriose douloureuse. Recommandation pour la pratique clinique : l’endométriose J Gynecol Obst Bio Reprod (Paris) 2007; 36: 141-50.
- 10. Roman H, Ness J, Suciu N, Bridoux V, Gourcerol G, et al. Are digestive symptoms in women presenting with pelvic endometriosis specific to lesion localizations? A preliminary prospective study. Hum Reprod 2012; 27:3440– 3449. Figure 7 : Choix thérapeutique en cas d’endométriose profonde douloureuse pour laquelle un traitement chirurgical est éventuellement indiqué Abrao MS Reproduction Update, 2015 Vol.21, No.3 pp. 329–339. 285 COLO PROCTOLOGIE
- 11. Lazzeri L, Di Giovanni A, Exacoustos C, Tosti C, Pinzauti S, et al. Preoperative and Postoperative Clinical and Transvaginal Ultrasound Findings of Adenomyosis in Patients With Deep Infiltrating Endometriosis. Reprod Sci. 2014 Aug;21(8):1027- 1033. Epub 2014 Feb 14. PMID: 24532217
- 12. Chapron C, Marcellin L, Borghese B, and Santulli P. Rethinking mechanisms, diagnosis and management of endometriosis. Nature Reviews Endocrinology https://doi.org/10.1038/ s41574-019- 0245-z
- 13. Roman H, Bourdel N, Hochain P, Opris I, Pirot N, et al. Endométriose colo-rectale diagnostic et traitement certitudes et interrogations – EMC (Elsevier Masson SAS, Paris), Gastroenterologie, 9-061- A-80, 2010.
- 14. Giudice LC, Telles TL, Lobo S, Kao L. The molecular basis for implantation failure in endometriosis: on the road to discovery. Ann N Y Acad Sci. 2002 Mar955:252-64; discussion 293-5, 396-406.
- 15. Boujenah J, Hugues JN, Sifer C, Bricou A, et al. Endometriosis Fertility Index or classification of the American Society of Reproductive Medicine for post operative endometriosis patients with infertility which is more relevant? Gynecol Obstet Fertil. 2015 Dec.43(12):806-9. doi: 10.1016/j.
- 16. Trippia CH, Zomer MT, Terazaki CR, Martin RL, Ribeiro R, et al. Relevance of Imaging Examinations in the Surgical Planning of Patients with Bowel Endometriosis. Clin Med Insights Reprod Health. 2016; 10: 1–8.
- 17. Desplats V, Vitte RL, Du Cheyron J, Roseau G, Fauconnier A, Moryoussef F. Preoperative rectosigmoid endoscopic ultrasonography predicts the need for bowel resection in endometriosis. World J Gastroenterol. 2019 Feb 14;25(6):696-706. doi: 10.3748/wjg. V 25. i6.696.
- 18. Chattot C, Huchon C, Paternostre A, Du Cheyron J, Chouillard E, et al. ENDORECT: a preoperative score to accurately predict rectosigmoid involvement in patients with endometriosis. Hum Reprod Open. 2019 Apr 3;2019(2): hoz 007. doi: 10.1093/hropen/ hoz007. Collection 2019.
- 19. Gauche Cazalis C, Koskas M, Martin B, Palazzo L, Madelenat P, et al. Preoperative imaging of deeply infiltrating endometriosis in: Transvaginal sonography, rectal endoscopic sonography and magnetic resonance imaging Gynecol Obstet Fertil 2012; 40: 634-41.
- 20. Chen YH, Wang DB, Guo CS. Accuracy of Physical Examination, Transvaginal Sonography, Magnetic Resonance Imaging, and Rectal Endoscopic Sonography for Preoperative Evaluation of Rectovaginal Endometriosis. Ultrasound Q. 2019 Mar;35(1):54-60. doi: 10.1097/RUQ.0000000000000428.
- 21. Abrao MS, Petraglia F, Falcone T, Keckstein J, Osuga Y, et al. Deep endometriosis infiltrating the recto-sigmoid: critical factors to consider before management. Human Deep endometriosis infiltrating the recto-sigmoid: critical factors to consider before management. Reproduction Update, Vol.21, No.3 pp. 329–339, 2015.
- 22. Bazot M, Daraï E. D i a g n o s i s of deep endometriosis: clinical examination, ultrasonography, magnetic resonance imaging, and other techniques. Fertil Steril. 2017 Dec;108(6):886-894. doi: 10.1016/j.fertnstert.2017.10.026.
- 23. Nisenblat V, Prentice L, Bossuyt PM, Farquhar C, Hull ML, et al. Combination of the non-invasive tests for the diagnosis of endometriosis. Cochrane Database Syst Rev. 2016 Jul 13;7:CD012281. doi: 10.1002/14651858.CD012281.
- 24. Alborzi S, Rasekhi A, Shomali Z, et al. Diagnostic accuracy of magnetic resonance imaging, transvaginal, and transrectal ultrasonography indeep infiltrating endometriosis. Medicine 2018: Feb; 97(8): e9536. Published online 2018 Feb 23. doi: 10.1097/ MD.0000000000009536 x.
- 25. Piketti MN, Chopin N, Dousset B, Millischer-Bellaische A, Roseau G, et al. Preoperative work-up for patients with deeply infiltrating endometriosis: transvaginal ultrasonography must definitely be the first-line imaging examination Human Reproduction, Volume 24, Issue 3, March 2009, Pages 602–607, https:// doi.org/10.1093/humrep/den405.
- 26. Holland TK, Cutner A, Saridogan E, Mavrelos D, Pateman K, and al. Ultrasound mapping of pelvic endometriosis: does the location and number of lesions affect the diagnostic accuracy? a multicentre diagnostic accuracy study BMC Womens Health. 2013; 13: 43. Published online 2013 Oct 29. doi: 10.1186/1472- 6874-13-43.
- 27. Rosefort A, Huchon C, Estrade S, Paternostre A, Bernard JP, et al. Is training sufficient for ultrasound operators to diagnose deep infiltrating endometriosis and bowel involvement by transvaginal ultrasound. J Gynecol Obstet Hum Reprod 2018 A^r 11.pii: S2468- 7847(17)30259-3.
- 28. Chapron C, Dumontier I, Dousset B, Fritel X, Tardif D, et al. Results and role of rectal endoscopic ultrasonography for patients with deep pelvic endometriosis Hum Reprod. 1998 Aug13(8): 2266-70.
- 29. Roseau G, Dumontier I, Palazzo L, Chapron C, Dousset B, et al. Rectosigmoid endometriosis endoscopic ultrasound features and clinical implications. Endoscopy. 2000 Jul;32(7):525-30.
- 30. Abrão MS, Neme RM, Averbach M, Petta CA, Aldrighi JM. Rectal endoscopic ultrasound with a radial probe in the assessment of rectovaginal endometriosis. J Am Assoc Gynecol Laparosc. 2004 Feb;11(1):50-4.
- 31. Delpy R, Barthet M, Gasmi M, Berdah S, Shojai R, et al. Value of endorectal ultrasonography for diagnosing rectovaginal septal endometriosis infiltrating the rectum. Endoscopy 2005; 37: 357-61.
- 32. Bahr A, De Parades V, Gadonneix P, Etienney I, Salet-Lizée D, et al. Endorectal ultrasonography in predicting rectal wall infiltration in patients with deep pelvic endometriosis: a modern tool for an ancient disease. Dis Colon Rectum 2006 Jun;49 (6):869-75.
- 33. Rossi L, Palazzo L, Yazbeck C, Walker F, Chis C, et al. Can rectal endoscopic sonography be used to predict infiltration depth in patients with deep infiltrating endometriosis of the rectum? Ultrasound Obstet Gynecol. 2014 Mar; 43(3): 322-7. doi: 10.1002/uog.12535.
- 34. James TW, Fan YC, Schiff L D , Gangarosa LM. Lower endoscopic ultrasound in preoperative evaluation of rectosigmoid endometriosis. Endosc Int Open. 2019 Jun;7(6): E837-E840. doi: 10.1055/a-0901-7259. Epub 2019 Jun 12.
- 35. Chapron C, Vieira M, Chopin N, Balleyguier C, Barakat H, et al. Accuracy of rectal endoscopic ultrasonography and magnetic resonance imaging in the diagnosis of rectal involvement for patients presenting with deeply infiltrating endometriosis. Ultrasound Obstet Gynecol. 2004 Aug;24(2):175-9.
- 36. Bazot M, Lafont C, Rouzier R, et al. Diagnostic accuracy of physical examination, transvaginal sonography rectal endoscopic ultrasonography and magnetic resonance imaging to diagnose deep infiltrating endometriosis Fertil Steril. 2009 Dec;92(6):1825-33.
À retrouver sur https://www.fmcgastro.org/wp-content/uploads/2020/05/277_020_Roseau.pdf
La FMC HGE a vu le jour en 1982 avec pour objectif de proposer une formation médicale continue pour tous les domaines que regroupent cette spécialité. La formation propose notamment 8 sessions plénières et 8 ateliers qui permettent d’aborder ses domaines de compétences au cours des Journées Francophones d’Hépatogastroentérologie et Oncologie Digestive.
Association Française de Formation Médicale Continue en Hépato-Gastro-Entérologie (FMCHGE)
