Endométriose colo-rectale : comment la traiter ?
Article
Publié le 16/05/2022
Information proposée par Association Française de Formation Médicale Continue en Hépato-Gastro-Entérologie (FMCHGE)
Les cinq points à retenir
- L’endométriose colorectale concerne environ 15 % des patientes atteintes d’endométriose profonde ; elle en est une forme particulière.
- Le diagnostic d’endométriose profonde et celui d’atteinte colorectale sont suspectés sur des signes cliniques ; ils doivent être confirmés par l’imagerie non invasive (échographie trans vaginale, IRM pelvienne, échoendoscopie rectale).
- Le retentissement peut être majeur sur la qualité de vie en raison des douleurs et de l’infertilité.
- La prise en charge repose avant tout sur le traitement médical ; elle doit être assurée par une équipe pluridisciplinaire, supervisée par un centre expert. La chirurgie est nécessaire en cas de lésions colorectales occlusives, d’absence d’efficacité des traitements médicaux, et de complications imposant un geste urgent ; la coelioscopie à visée purement diagnostique est à déconseiller.
- L’échoendoscopie rectale peut être utile au diagnostic d’atteinte colo-rectale ; elle s’intègre dans le cadre d’un bilan préopératoire.
Traitement
La prise en charge l’endométriose colo-rectale est indissociable de celle de l’endométriose profonde qui est, de toutes les formes d’endométriose, la plus invalidante et la plus difficile à traiter. En règle générale, le traitement est d’autant plus efficace que le diagnostic d’endométriose profonde a été précocement porté et devrait rester médical pour la plus grande partie des femmes concernées (12, 40).
En dehors de situations aiguës graves (fonction rénale menacée par une obstruction urétérale, ou autre complication nécessitant une intervention chirurgicale urgente…), ce n’est qu’au terme d’un examen clinique soigneux, et d’un bilan d’extension para-clinique complet, qu’une stratégie particulière peut être raisonnablement proposée et décrite en détail aux patientes (21). Il convient de bien leur expliquer le schéma du traitement retenu, ses objectifs, et les risques de complications qu’il peut faire courir : échec, intolérance, ou effet d’échappement des traitements médicamenteux, morbidité post-opératoire, et même récidive toujours possible, y compris même après chirurgie radicale (41). Cela est particulièrement important dans les formes avec une atteinte colo-rectale qui rend le traitement chirurgical plus complexe et plus risqué.
Les traitements médicamenteux peuvent avoir une efficacité symptomatique en agissant sur la composante inflammatoire mais ils n’ont pas d’effet sur la fibrose constituée, expliquant leur faible effet en cas de dyspareunie et/ou de signes digestifs en lien avec une sténose constituée. De plus ces traitements ne sont que « suspensifs » et n’excluent pas la progression de l’atteinte digestive même si l’aménorrhée est maintenue (42). Ces éléments expliquent le recours parfois incontournable à la chirurgie (situations d’urgence, contre-indication et échec des traitements médicaux…).
Les traitements médicaux
Endométriose profonde, principaux traitements médicaux
- Traitements antalgiques et anti-inflammatoires non stéroïdiens
- Traitements hormonaux
- Contraceptions estroprogestatives (efficaces et bien tolérées pour traiter les multiples formes d’endométriose ; administration en mode continu préférable).
- Progestatifs (macro ou micro, ou système intra-utérin au lévonorgestrel (efficaces et bien tolérées).
- Agonistes la GnRH : décapeptides de synthèse (pas plus efficaces que les autres traitements hormonaux et sources d’effets secondaires hypoestrogéniques pouvant être atténués par une hormonothérapie de substitution. Effet délétère sur la densité osseuse contre indiquant un usage prolongé).
- Autres :
- Validés : antagonistes de la GnRH, Danazol
- Non validés, mais faisant l’objet de travaux de recherche clinique : anti-aromatases, modulateurs sélectifs des récepteurs à la progestérone, anti-TNF alpha, inhibiteurs des métalloprotéases…
Ils sont proposés à des patientes symptomatiques, et peuvent être suffisants à eux seuls ou bien venir en complément de la chirurgie (préparation à une intervention, ou traitement post-opératoire…). Aujourd’hui, plusieurs molécules sont couramment prescrites qu’il s’agisse des anti-inflammatoires non stéroïdiens et des antalgiques, ou des traitements hormonaux(40, 42, 43). Ceux-ci ne sont pas utilisables chez les patientes qui souhaitent débuter une grossesse, ou qui présentent des contre-indications (terrain d’accident vasculaire, d’angiomes et/ou de risque de néoplasie génitale).
Les œstro-progestatifs ou les progestatifs seuls qui induisent une aménorrhée sont prescrits en première ligne avec des résultats analogues sur les douleurs, mais aussi en partie sur les symptômes digestifs. La plupart des études comparant le traitement hormonal, lorsqu’il est bien toléré, à l’abstention ou la prise d’un placébo, montrent une baisse significative des douleurs (43). Les agonistes de la GnRH peuvent également être proposés, mais ils ne doivent être utilisés que pendant une période limitée puisque leur usage prolongé peut générer des risques de déminéralisation osseuse grave. D’autres molécules sont d’usage moins courant (antagonistes de la GnRH, Danazol), ou encore au stade d’essais cliniques (anti-aromatase, inhibiteurs des métalloprotéases…).
Pour certaines patientes, l’utilisation à visée symptomatique des mêmes traitements que ceux habituellement proposés dans le syndrome de l’intestin irritable est possible, comme le recours pour d’autres, à des anxiolytiques ou des antidépresseurs. Signalons enfin que l’accompagnement dans le cadre de consultations de suivi, et parfois la prescription d’une psychothérapie, font partie intégrante de la prise en charge de l’endométriose tout au long de son évolution.
Traitement chirurgical (40, 44-50)
Le « moment » de la chirurgie et son type doivent idéalement être appropriés à chaque patiente, et l’intervention doit être réalisée en milieu pluridisciplinaire spécialisé. L’intervention vise le geste optimal adapté aux symptômes à traiter (douleur et/ou infertilité), avec la morbidité la plus basse, en évitant le recours aux interventions itératives, véritable marqueur de gravité (chaque intervention devient plus complexe et source d’un plus fort taux de complication).
Longtemps considérée comme le traitement de choix des patientes ayant une endométriose profonde avec atteintes digestives (47), la chirurgie surtout lorsqu’elle est radicale n’est cependant jamais exempte de risque de complications précoces ou plus tardives ; de plus, l’apparition post-opératoire de troubles fonctionnels qui n’existaient pas au préalable et la récidive restent toujours possibles (41, 48-50).
Après des années d’affrontement entre les partisans de la chirurgie ouverte et ceux de la cœlioscopie est apparu un autre débat opposant deux conceptions d’exérèses digestives : radicale ou conservatrice. En pratique, les patientes ayant une endométriose profonde avec atteinte colo-rectale se voient proposer trois types d’intervention dont l’analyse des résultats fonctionnels et de la morbidité font l’objet de nombreuses publications.
La résection segmentaire (48, 49) est l’intervention la plus ancienne et celle qui, jusqu’à une période récente, avait été la plus étudiée. Plus standardisée et davantage pratiquée que la résection discoïde (dite aussi nodulectomie), elle est grevée d’un taux incompressible de complications. Par ailleurs, elle est souvent redoutée des patientes, en raison de la possibilité d’une colostomie transitoire. Elle connaît aujourd’hui un net recul pour ces raisons, mais aussi et surtout parce que les interventions plus conservatrices (shaving notamment), lorsqu’elles sont réalisables, offrent des résultats fonctionnels en termes de douleurs, infertilité, et qualité de vie, au moins aussi bons, et avec une moindre morbidité. En outre la pertinence du concept de radicalité est battue en brèche par le fait qu’une intervention conservatrice peut être complétée d’un traitement médical, et qu’une deuxième intervention radicale peut être proposée plus tardivement à une femme ayant surmonté son infertilité et/ou atteint l’âge de la ménopause. Elle garde cependant des indications : patientes ne pouvant pas bénéficier d’un traitement médical continu, ou non améliorées en pré-opératoire par celui-ci, symptômes digestifs prédominants (sub-occlusion), âge jeune et désir de fertilité. Elle s’impose enfin en cas de lésion rectale étendue, d’infiltration sigmoïdienne, ou de lésions multiples.
Le shaving est un « pelage » de la paroi antérieure du rectum infiltrée par le nodule profond au contact. Cette technique entraîne peu de complications et, à son décours, il y a peu ou pas de patientes aggravées notamment par la survenue de symptômes digestifs « de novo ». Elle n’a que très peu d’effet sur la constipation et son taux de récidive est probablement plus élevé que celui observé après résection segmentaire (5-10 %). Le shaving est donc destiné aux patientes non désireuses d’une grossesse même à long terme, qui peuvent bénéficier d’un traitement médical continu, et dont les symptômes ont été améliorés par celui-ci en pré-opératoire (45, 46). Il peut donc se définir comme un bon traitement de première ligne des nodules de moins de 2 cm de diamètre ou de 2 à 4 cm sans atteinte de la sous-muqueuse (bonne indication des nodules de la séreuse ou musculeuse de moins de 2 cm et sans développement net sur la circonférence), mais il ne peut pas être réalisé en cas de lésion sigmoïdienne. Il est parfois la première étape d’un traitement en deux temps.
La nodulectomie dont la résection discoïde est la version la plus usitée, et d’autres techniques en cours d’évaluation, sont plus rarement réalisées (46). Parmi les inconvénients de la résection discoïde, il faut compter la difficulté des sutures et un taux de fistules proche de celui des résections segmentaires, mais aussi le taux élevé de résections microscopiques incomplètes. Elle concernerait théoriquement les patientes avec des atteintes de taille intermédiaire limitée dans l’épaisseur de la musculeuse et sur la circonférence, et qui ne sont pas améliorées par le traitement médical pré opératoire ou ne peuvent pas bénéficier d’un traitement continu, tout en ayant un désir de fertilité.
Les indications respectives de ces interventions, tout comme la question récurrente « faut-il ou ne faut-il pas opérer ? », sont quotidiennement débattues, et deux situations particulières peuvent illustrer la complexité de ce choix. La première serait le cas d’une patiente jeune ayant de lourdes complications ou des symptômes invalidants apparus après chirurgie radicale. L’autre correspondrait à une abstention chirurgicale prolongée au profit d’un traitement médical long, notamment pour infertilité, et donnant lieu au fil des années à une aggravation, privant la patiente d’une chirurgie conservatrice qui aurait été possible si elle avait été envisagée plus précocement. L’adage « chirurgie raisonnée, ni trop hâtive, ni trop tardive » se justifie donc pleinement. L’endométriose peut s’aggraver même sous traitement hormonal (42). Le traitement médical n’est que suspensif, donc si on choisit de ne pas opérer, il faut insister sur l’importance d’un suivi médical régulier.
Les indications thérapeutiques dépendent de nombreux facteurs :
1/ propres à la patiente (histoire clinique et souhaits de la patiente particulièrement en termes de grossesse, pathologies associées, symptômes, traitements contre-indiqués ou déjà réalisés…)
2/ en rapport avec l’anatomie lésionnelle (taille, nombre, localisation sur le rectum et/ou le sigmoïde)
3/ liés à la cinétique d’évolution de la lésion qui n’est que très rarement linéaire. L’usage actuel suggère une prise en charge graduée commençant par les thérapeutiques les moins morbides, tant pour le traitement des douleurs que pour celui de l’infertilité.
Un des schémas les plus consensuels désormais est celui du recours premier à un traitement médical optimal des symptômes (douleurs et infertilité surtout, troubles digestifs et urinaires fonctionnels), la chirurgie sous la forme d’une exérèse radicale avec hystérectomie, venant en seconde intention parfois même à l’approche de la ménopause ou une fois celle-ci avérée.
Cette prise en charge sur le long terme justifie des consultations spécialisées régulières, avec une appréciation objective possible des douleurs, utilisant les Échelles Visuelles Analogiques. Le shaving tend à être le plus souvent proposé du fait de bons résultats sur le contrôle des douleurs, la fertilité, et la qualité de vie, au prix d’un risque théorique plus élevé de récidives, celles-ci pouvant être traitées médicalement et/ou donner lieu à une seconde intervention plus à distance.
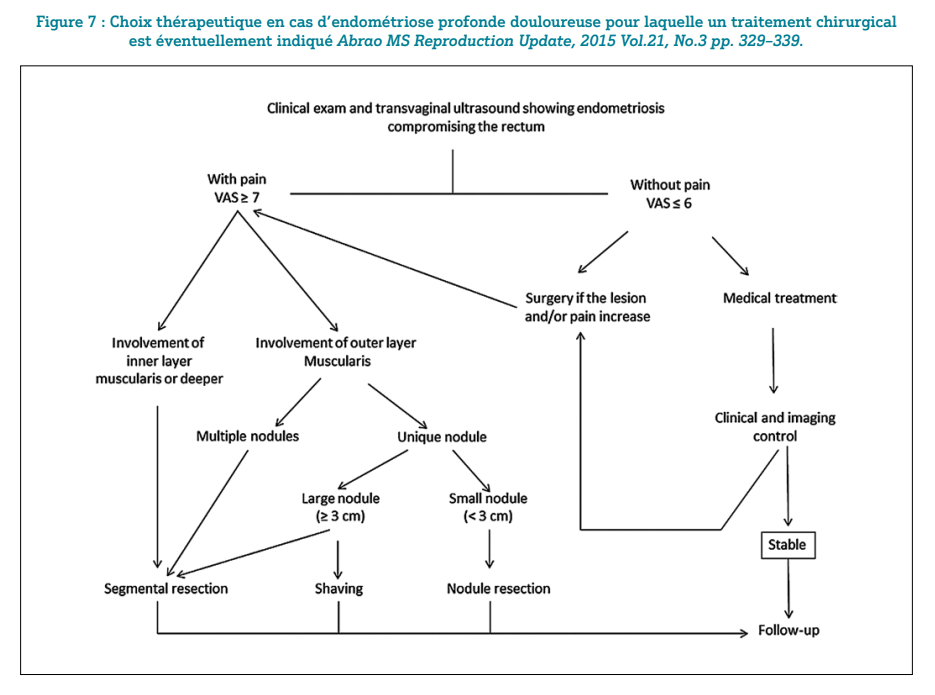
Pour les patientes chez lesquelles les douleurs sont prépondérantes, les orientations thérapeutiques sont résumées dans l’algorithme (figure 7). Lorsque même en présence d’une atteinte colo-rectale, l’infertilité est le problème principal, il a été admis que la PMA pouvait donner de bons résultats sous réserve de l’absence de facteurs péjoratifs : adénomyose associée, taux abaissé d’hormone anti-mullérienne, et âge supérieur à 35 ans.
En règle plus générale, chez de jeunes patientes infertiles, la chirurgie peut aussi être proposée précocement ou s’imposer après deux échecs de FIV (53)
Conclusion
La localisation la plus fréquente de l’endométriose digestive est l’infiltration colo-rectale, elle peut compliquer l’endométriose profonde dans 15 % des cas environ. Elle se définit histologiquement pas l’infiltration de la musculeuse digestive et s’accompagne de difficultés en terme de diagnostic clinique justifiant un interrogatoire et un examen clinique rigoureux et le recours facile à l’imagerie.
Si l’ETV tend à devenir l’examen de première ligne, l’IRM et l’EER sont utiles chez les patientes pour lesquelles un traitement chirurgical est envisagé.
Les recherches cliniques en cours tendent à définir un véritable « phénotypage » de l’endométriose, afin de la diagnostiquer précocement et d’optimiser les traitements avec une option médicale privilégiée et un recours à la chirurgie limitée aux indications incontournables (12).
Test de connaissances
Nous vous invitons à tester vos connaissances sur l’ensemble des QCU (Questionnaire à Choix Unique) de www.fmcgastro.org : testez ici vos connaissances sur le sujet.
Références
- 12. Chapron C, Marcellin L, Borghese B, and Santulli P. Rethinking mechanisms, diagnosis and management of endometriosis. Nature Reviews Endocrinology https://doi.org/10.1038/ s41574-019- 0245-z
- 21. Abrao MS, Petraglia F, Falcone T, Keckstein J, Osuga Y, et al. Deep endometriosis infiltrating the recto-sigmoid: critical factors to consider before management. Human Deep endometriosis infiltrating the recto-sigmoid: critical factors to consider before management. Reproduction Update, Vol.21, No.3 pp. 329–339, 2015.
- 40. Giudice LC, Kao LC. Endométriosis. Lancet. 2004 Nov 13-19;364(9447): 1789-99. Review.
- 41. Nirgianakis K, McKinnon B, Imboden S, Knabben L, Gloor B, et al. Laparoscopic management of bowel endometriosis: resection margins as a predictor of recurrence. Acta Obstet Gynecol Scand 2014; 93:1262-67.
- 42. Millochau JC, Abo C, Darwish B, Huet E, Dietrich G, et al. Continuous Amenorrhea May Be Insufficient to Stop the Progression of Colorectal Endometriosis. J Minim Invasive Gynecol. 2016 Jul-Aug;23(5):839-42. doi: 10.1016/j. jmig.2016.04.008. Epub 2016 Apr 26.
- 43. Azoulay C, Bardy C, Lassere M, Brun JL. Traitements médicamenteux de l’endométriose (adénomyose exclue). EMC (150-A-15) Doi: 10.1016/ S024661064(17)67531-5.
- 44. Abou-Setta AM, Houston B, Al-Inany HG, Farquhar C. Levonorgestrel-releasing intrauterine device (LNG_IUD) for symptomatic endometriosis following surgery, Cochrane Database Syst Rev. 2013 Jan 31;(1):CD005072. doi: 10.1002/14651858. CD005072.pub3. Review. 286
- 45. Donnez O, Roman H. Choosing the right surgical technique for deep endometriosis: shaving, disc excision, or bowel resection? Fertil Steril. 2017 Dec;108(6):931-942. doi: 10.1016/j.fertnstert.2017.09.006.
- 46. Roman H, Vassilieff M, Gourcerol G, Savoye G, Leroi AM, et al. Surgical management of deep infiltrating endometriosis of the rectum: pleading for a symptom-guided approach. Hum Reprod. 2011 Feb;26(2):274-81. doi: 10.1093/humrep/deq332. Epub 2010 Dec 2.39
- 47. Dousset B, Leconte M, Borghese B, Millischer AE, Roseau G, Arkwright S, Chapron C. Complete surgery for low rectal endometriosis: long-term results of a 100-case prospective study… Ann Surg. 2010 May;251(5):887-95. doi: 10.1097/ SLA.0b013e3181d9722d.
- 48. Bourdel N, Comptour A, Bouchet P, Gremeau AS, Pouly JL, et al. Long-term evaluation of painful symptoms and fertility after surgery for large rectovaginal endometriosis nodule: a retrospective study. Acta Obstet Gynecol Scand. 2018 Feb;97(2): 158-167.
- 49. Bassi MA, Podgaec S, Dias JA Jr, D’Amico Filho N, Petta CA, et al. Quality of life after segmental resection of the rectosigmoid by laparoscopy in patients with deep infiltrating endometriosis with bowel involvement. J Minim Invasive Gynecol 2011;18:730–733.
- 50. Kondo W, Bourdel N, Tamburro S, Cavoli D, Jardon K, et al. Complications after surgery for deeply infiltrating pelvic endometriosis. BJOG 2011; 118: 292–298.
- 51. Soto E, Catenacci M, Bedient C, Jelovsek JE, Falcone T. Assessment of Long-Term Bowel Symptoms After Segmental Resection of Deeply Infiltrating Endometriosis: A Matched Cohort Study. J Minim Invasive Gynecol. 2016 Jul-Aug;23(5):753-9. doi: 10.1016/j. jmig.2016.03.004. Epub 2016 Mar 11.
- 52. Sibiude J, Santulli P, Marcellin L, Borghese B, Dousset B, et al. Association of history of surgery for endometriosis with severity of deeply infiltrating endometriosis. Obstet Gynecol. 2014 Oct;124(4):709-17. doi: 10.1097/ (13).
- 53. Ballester M, d’Argent EM, Morcel K, Belaisch-Allart J, Nisolle M, et al. Cumulative pregnancy rate after ICSI-IVF in patients with colorectal endometriosis: results of a multicentre study. Hum Reprod 2012; 27:1043-1049.
À retrouver sur https://www.fmcgastro.org/wp-content/uploads/2020/05/277_020_Roseau.pdf
La FMC HGE a vu le jour en 1982 avec pour objectif de proposer une formation médicale continue pour tous les domaines que regroupent cette spécialité. La formation propose notamment 8 sessions plénières et 8 ateliers qui permettent d’aborder ses domaines de compétences au cours des Journées Francophones d’Hépatogastroentérologie et Oncologie Digestive.
Association Française de Formation Médicale Continue en Hépato-Gastro-Entérologie (FMCHGE)